纳米代谢组学揭示3D打印血管支架的生物响应与代谢奥秘
心血管疾病已成为发达国家导致死亡和残疾的主要原因,血管支架是治疗心血管狭窄的有效手段。传统方法制造的标准支架,因形态异质性、稳定性和生物相容性欠佳,容易引发血栓形成和心肌梗死等问题。3D打印技术为构建个性化血管支架带来新希望,3D打印血管支架(3D-PVS)能依据患者血管结构定制,优化机械性能,拓展临床适应症。然而,目前3D-PVS的生物相容性分析仅停留在表型层面,其深层分子机制亟待探索,这限制了3D-PVS的临床应用。
四川大学华西医院的关俊文、张定坤教授团队运用纳米代谢组学技术,对3D-PVS的生物响应及相关分子机制展开研究。他们通过对细胞模型(人脐静脉内皮细胞)进行非靶向纳米代谢组学分析,初步探究3D-PVS对细胞代谢的影响;再基于此对大鼠模型进行靶向纳米代谢组学研究,深入探索3D-PVS诱导的代谢重编程。 相关工作以“Nanometabolomics elucidated biological response of 3D printed vascular stents: Towards metabolic reprogramming of metabolome and lipidome”为题发表在《Chemical Engineering Journal》上,为3D-PVS的临床应用提供了重要的理论和技术支持。

研究内容
1. 3D-PVS诱导代谢重编程的研究流程构建
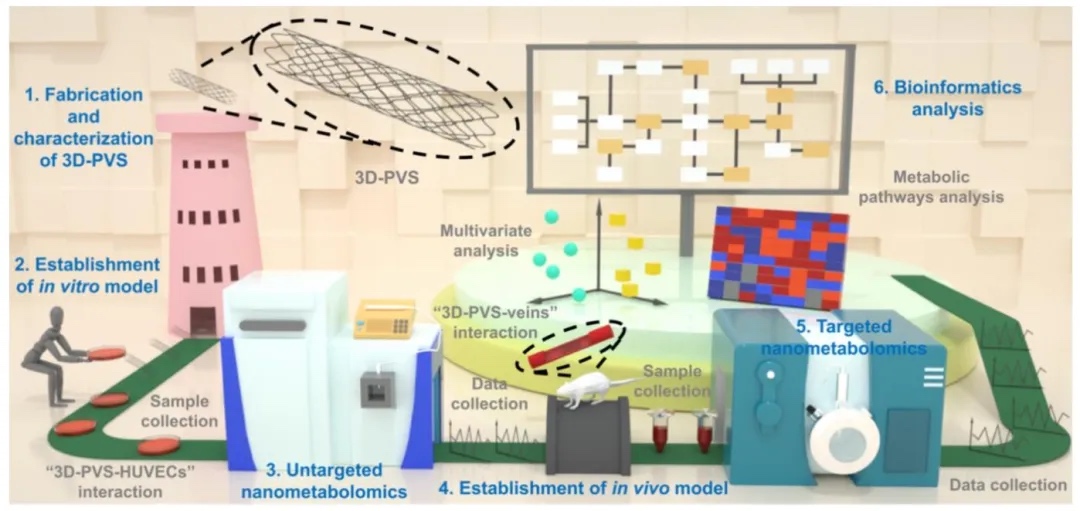
通过规划并展示一系列实验步骤,研究如何借助纳米代谢组学技术来探究3D-PVS诱导的代谢重编程机制。结果显示,该研究流程涵盖3D-PVS的制备与表征、体外和体内模型的构建、非靶向和靶向纳米代谢组学分析以及生物信息学分析等关键环节,为深入探究3D-PVS植入引发的代谢重编程分子机制搭建了合理框架。
2. 3D-PVS的结构表征
运用扫描电子显微镜(SEM)对3D-PVS进行观察,研究其微观结构特征。结果表明,3D-PVS呈现出空心圆柱微晶格结构,具备负泊松比(NPR)特性。这种结构不仅增强了支架的韧性,还显著提升了其径向支撑力和抗压性。同时,3D打印技术赋予3D-PVS规则且紧密排列的微观结构,有助于满足临床个性化治疗需求。

3. 基于HUVECs模型评估3D-PVS的生物相容性
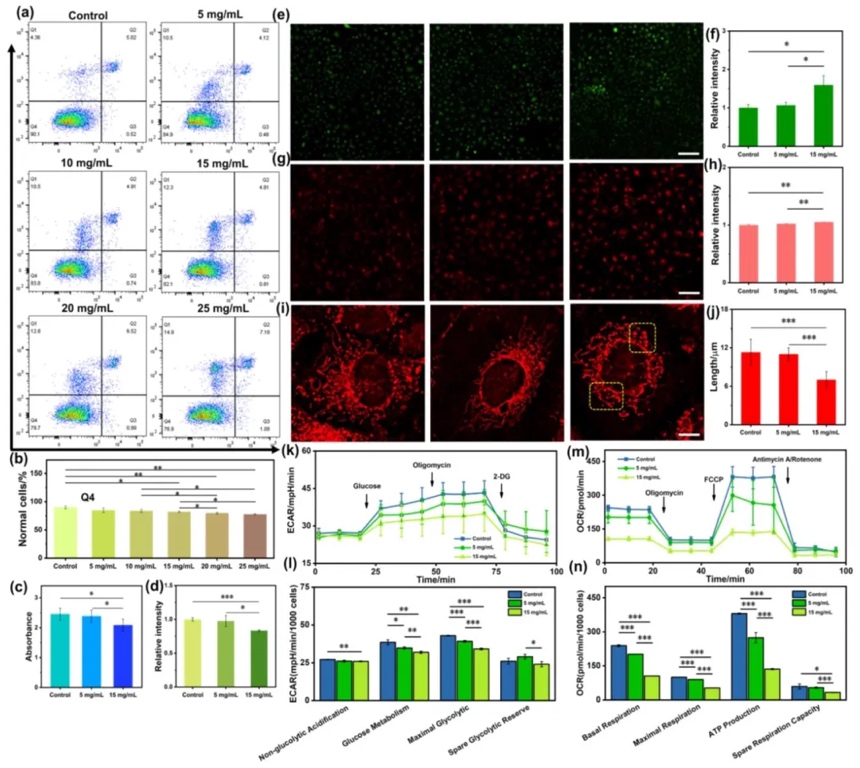
采用细胞凋亡检测、细胞活力检测、荧光成像以及海马细胞外流量分析等多种方法,以人脐静脉内皮细胞(HUVECs)为模型,研究3D-PVS的生物相容性。结果显示,低浓度(5mg/mL)和高浓度(15mg/mL)的3D-PVS在一定程度上具有较好的生物相容性。不过,15mg/mL的3D-PVS会促使细胞内活性氧(ROS)产生和积累,抑制葡萄糖摄取与利用。但总体而言,在安全浓度范围内,3D-PVS的ROS相关毒性较低,对细胞的影响在可接受范围内。
4. 非靶向水性代谢组学研究
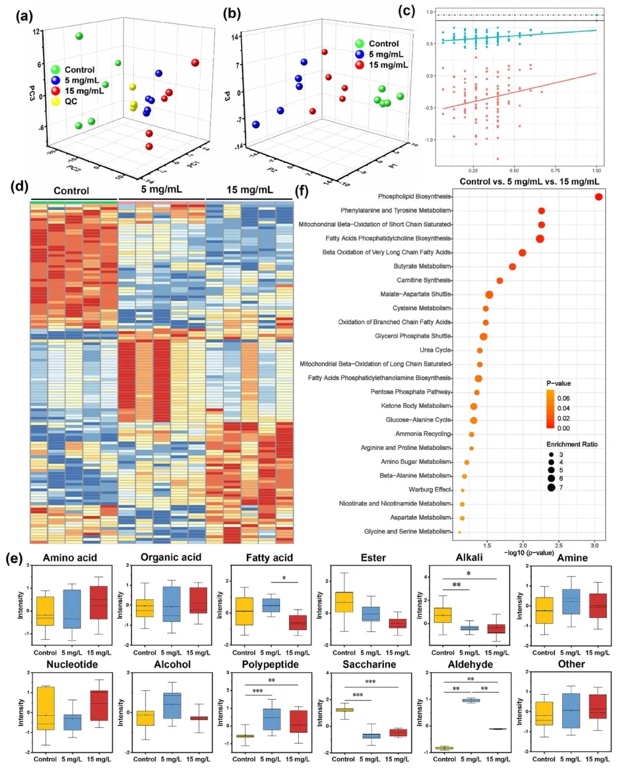
利用LC-MS/MS系统进行非靶向水性代谢组学分析,研究3D-PVS处理后的HUVECs在代谢层面的变化。结果发现,5mg/mL和15mg/mL的3D-PVS处理组与对照组相比,在代谢组水平上存在显著差异。共鉴定出123种差异代谢物,这些代谢物涉及氨基酸、有机酸和脂肪酸等多个代谢途径。其中,15mg/mL的3D-PVS诱导的代谢变化更为明显,体现出一定的剂量依赖性。
5. 非靶向脂质组学研究
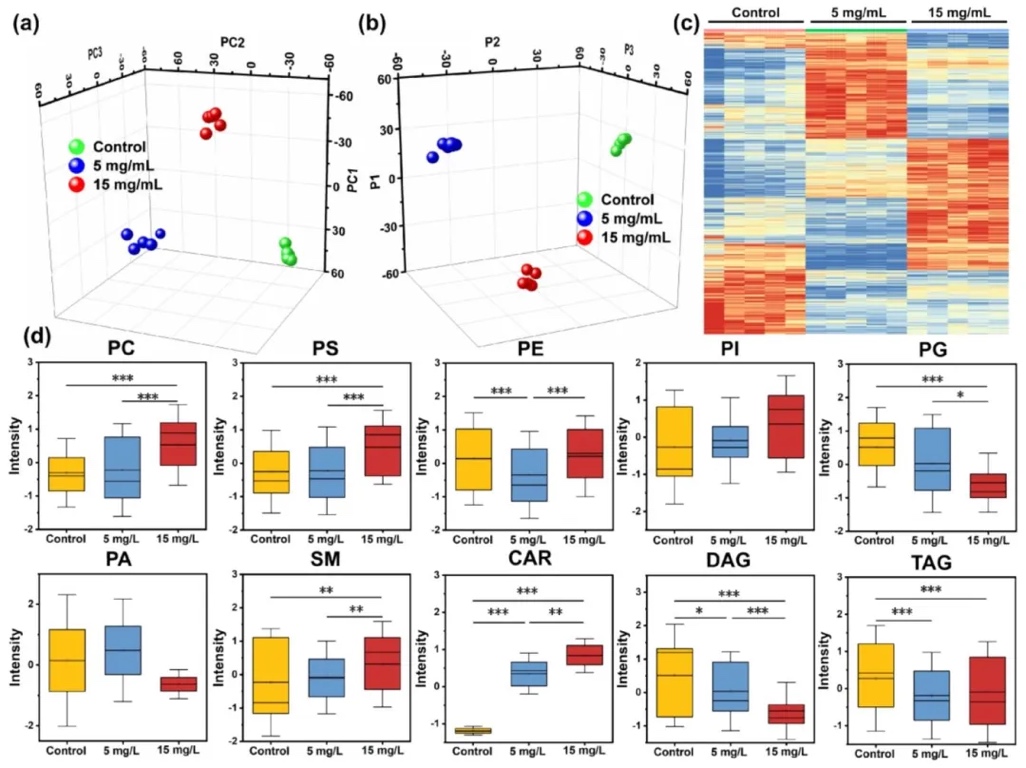
借助LC-MS/MS系统开展非靶向脂质组学分析,探究3D-PVS处理后HUVECs的脂质组变化情况。结果表明,3D-PVS处理组与对照组在脂质组水平上呈现出明显差异,共检测到2585种差异脂质,分属于26个脂质类别。15mg/mL的3D-PVS对差异脂质水平的干扰程度大于5mg/mL的3D-PVS,5mg/mL的3D-PVS也对脂质组产生了一定影响,进一步证实了3D-PVS与细胞相互作用的剂量依赖性。
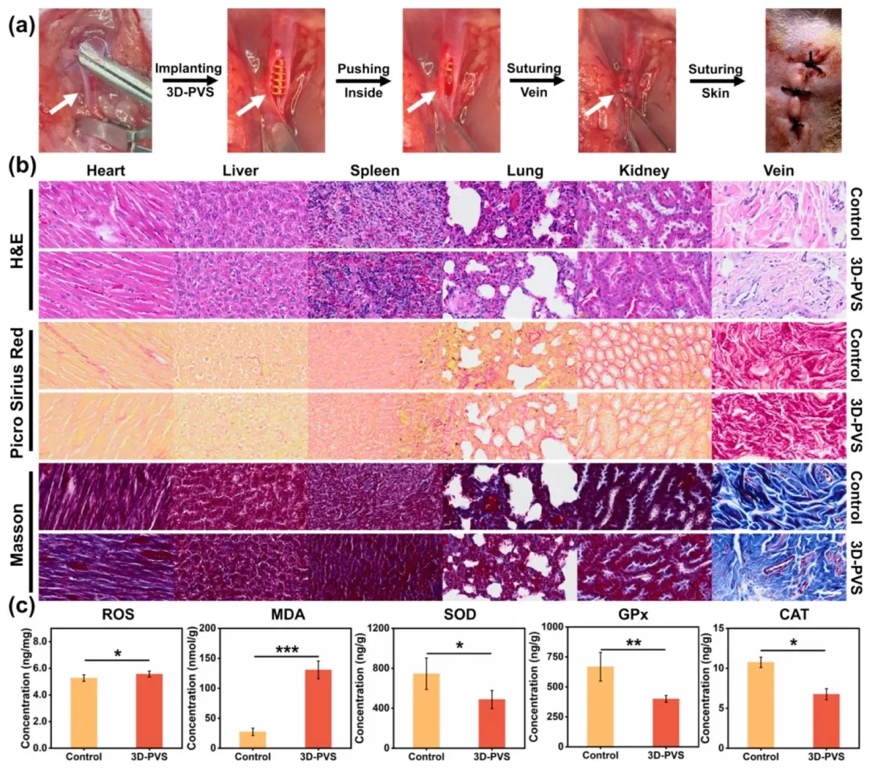
6. 体内模型的病理、成像和生化研究
通过建立大鼠体内模型,对植入3D-PVS后的大鼠进行病理染色,并检测氧化应激相关生物标志物,研究3D-PVS植入对大鼠体内的影响。结果显示,3D-PVS在体内表现出较好的生物相容性,未引起主要组织明显的形态学差异。然而,植入3D-PVS会导致大鼠体内产生一定程度的氧化应激,具体表现为ROS和丙二醛(MDA)水平升高,而超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GPx)和过氧化氢酶(CAT)等抗氧化酶的水平下降。
7. 靶向水性代谢组学研究
运用LC-MS/MS技术进行靶向水性代谢组学分析,研究3D-PVS植入后大鼠静脉的代谢变化。结果表明,3D-PVS植入显著影响了静脉中的糖酵解和氨基酸代谢过程。其中,糖酵解过程增强,同时色氨酸、蛋氨酸和半胱氨酸等多种氨基酸代谢途径发生波动。这些代谢变化有助于细胞抵抗3D-PVS植入引发的氧化应激、炎症反应和免疫排斥,维持代谢稳态。

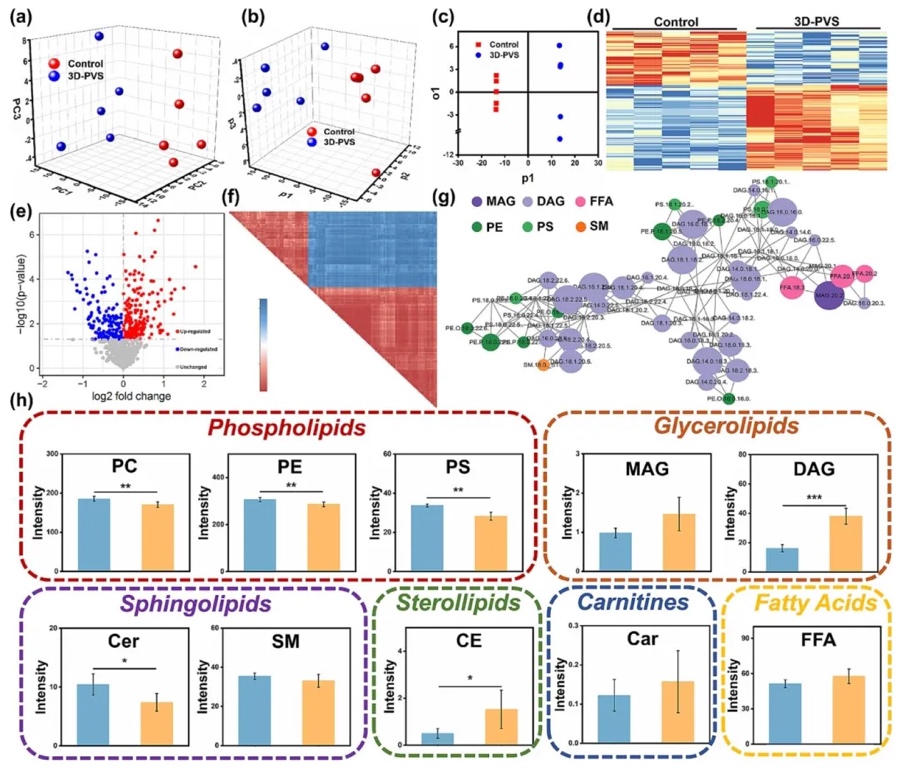
8. 靶向脂质组学研究
借助LC-MS/MS技术进行靶向脂质组学分析,探究3D-PVS植入后大鼠静脉的脂质代谢变化。结果发现,3D-PVS植入导致静脉中磷脂(如PC、PE和PS)水平升高,脂肪酸水平也相应上升,甘油三酯(如MAG和DAG)和胆固醇酯(CE)水平增加,鞘脂(如Cer和SM)水平下降,肉碱(Car)水平升高。这表明3D-PVS植入引发了脂质代谢的改变,使脂质代谢倾向于能量储存,同时对细胞的正常凋亡过程产生了一定干扰。
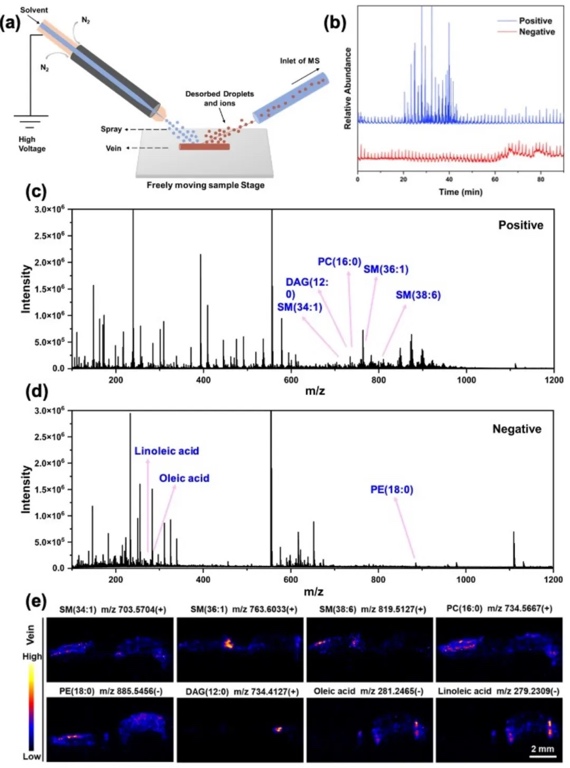
9. 空间代谢组学研究
采用解吸电喷雾电离质谱成像(DESI-MSI)技术,研究3D-PVS处理后大鼠静脉中差异代谢物的相对丰度和空间分布。结果显示,3D-PVS处理导致部分脂质(如SM(34:1)、SM(36:1)、SM(38:6)、PC(32:0)、PE(41:4)和DAG(35:4))水平下降,而脂肪酸(如油酸和亚油酸)水平升高。这一结果与靶向代谢组学和脂质组学的研究结果相符,进一步证实了3D-PVS会引起差异代谢物和脂质的重编程。
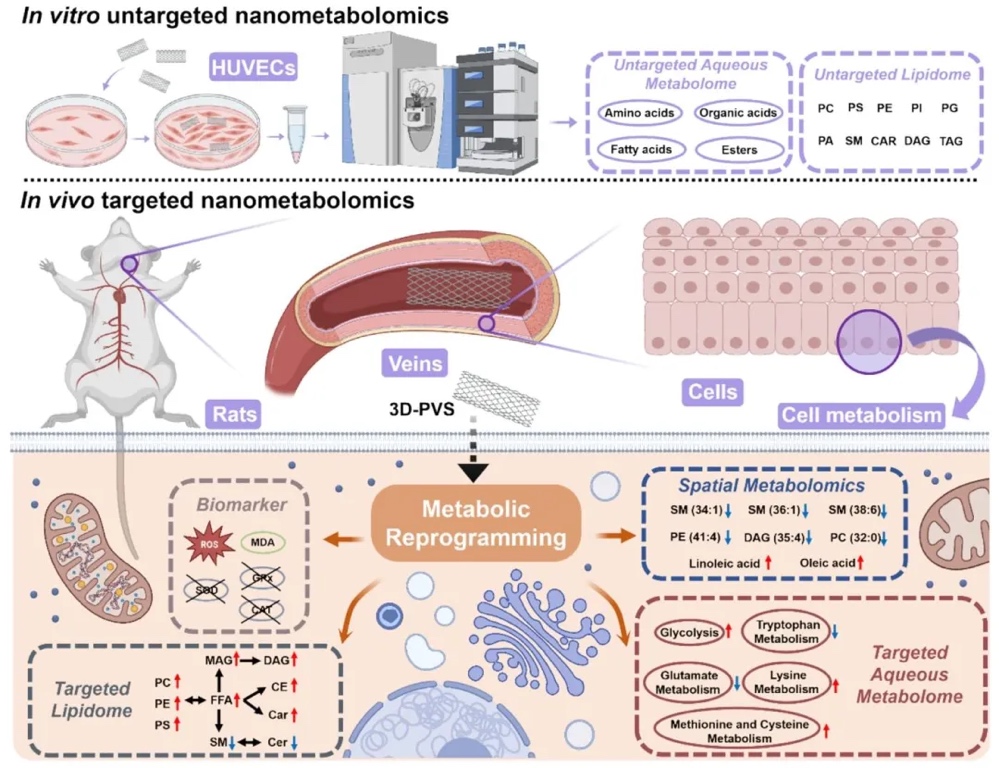
10. “3D-PVS-生物体”相互作用的生物事件示意图
通过整合各项实验结果绘制示意图,研究3D-PVS与生物体相互作用过程中的生物事件。结果表明,体外非靶向纳米代谢组学显示3D-PVS影响细胞代谢相关途径;体内靶向纳米代谢组学揭示3D-PVS诱导代谢重编程,涉及糖酵解、氨基酸代谢和脂质代谢等;空间代谢组学展示了差异脂质的空间分布变化。这些结果共同揭示了3D-PVS在生物体内的作用机制和代谢影响。
研究结论
本研究利用纳米代谢组学(包括非靶向/靶向水性代谢组学、脂质组学和空间代谢组学)阐释了3D打印血管支架(3D-PVS)的生物响应。这是首次运用纳米代谢组学方法,从代谢层面研究3D-PVS生物效应,并获取多维度生物信息。研究结果显示,3D-PVS在体外的安全浓度(<15mg/mL)会影响氨基酸或有机酸相关代谢,以及磷脂、鞘脂或甘油酯相关代谢。体内研究发现,3D-PVS能促进糖酵解和氨基酸代谢(包括色氨酸、半胱氨酸和甲硫氨酸、谷氨酸和赖氨酸代谢),并调节部分脂质类别(如PC、PE、PS、MAG、DAG、Cer、SM、CE、Car和FFA)的稳态。该研究为3D-PVS在生化、医学和工业领域的应用和发展提供了新视角,同时推动了纳米代谢组学在阐释3D打印纳米材料生物医学干预机制方面的技术和方法进步。
挑战与展望
尽管本研究借助纳米代谢组学对3D打印血管支架(3D-PVS)的生物响应有了深入了解,但仍面临挑战。在代谢机制方面,虽然明确了3D-PVS对代谢途径的影响,但具体分子调控网络还不够清晰,关键代谢节点的上下游调控关系有待进一步挖掘。从临床转化角度看,本研究仅在细胞和大鼠模型上进行,距离临床实际应用还有差距,不同个体间的差异可能导致3D-PVS的代谢响应不同,如何将研究成果精准应用于临床是一大难题。 展望未来,一方面可深入探究3D-PVS影响代谢的分子调控细节,构建完整的调控网络模型,为理解其生物效应提供更坚实的理论基础。另一方面,加强与临床医学的合作,开展更多人体相关研究,评估3D-PVS在不同人群中的代谢响应差异,推动其从实验室走向临床应用,为心血管疾病治疗带来新突破。
文章来源:
https://doi.org/10.1016/j.cej.2025.161051
(责任编辑:admin)


 嫦娥八号将在月球上3D打印
嫦娥八号将在月球上3D打印 香港科技大学开发人工智能
香港科技大学开发人工智能 Continuum Powders等离子
Continuum Powders等离子 西安交大张留洋教授课题组
西安交大张留洋教授课题组 多伦多大学邹宇团队增材制
多伦多大学邹宇团队增材制 《Small Science
《Small Science 南洋理工-剑桥大
南洋理工-剑桥大 清华大学:抗拉强
清华大学:抗拉强 《Science》:一
《Science》:一 国产大尺寸陶瓷3D
国产大尺寸陶瓷3D 南京工业大学:基
南京工业大学:基

