四军大与北大联合研究:3D打印表面活化镁离子的多孔聚醚醚酮支架(2)
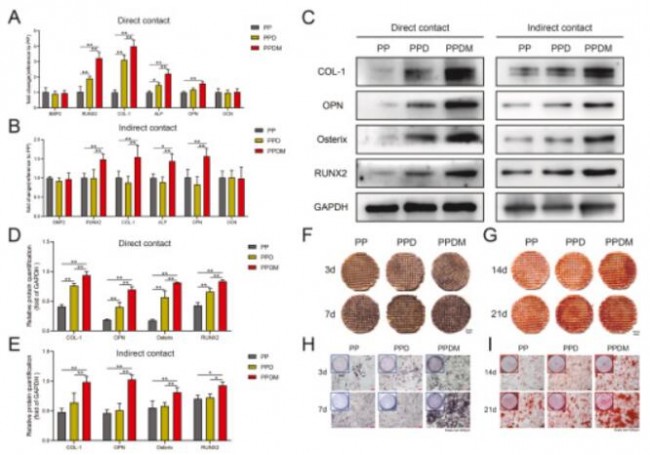
再次,进行了支架的MC3T3-E1成骨分化实验(图6)。首先在转录水平中,直接接触共培养后PPDM和PPD组Runx2、Col1和Alp基因的表达显著上调,而间接接触共培养PPDM组中的Runx2、Col1、Alp和Opn基因与其他两组相比上调。其次灰度分析表明,各培养状态下PPDM中COL1、OPN、Osterix和RUNX2的相对蛋白表达水平均高于其余两组。
最后,在碱性磷酸酶和茜素红染色中发现PPDM组中ALP表达与矿化结节含量均高于其余两组。自此,作者从成骨细胞在骨形成中的三个主要阶段(成骨细胞的黏附和增殖、成骨分化和细胞外基质矿化)多角度证明了该材料具有促进细胞成骨分化和成骨细胞矿化的作用。
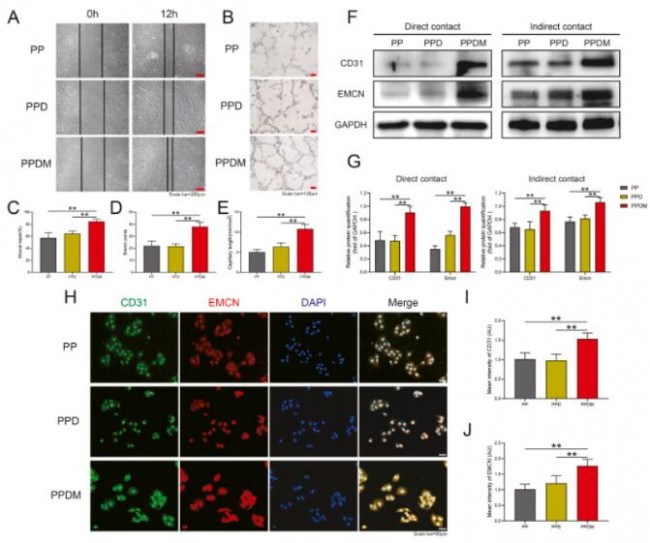
然后进行了HUVECs的迁移和血管生成实验(图7)。细胞划痕实验及血管形成实验证明PPDM组与其余样品相比具有促进细胞迁移和血管生成的功能。蛋白水平实验中,对血管标记CD31和EMCN进行Western blotting及免疫荧光染色实验,发现PPDM相关蛋白表达含量显著高于其余样品。证明PPDM有助于血管生成。
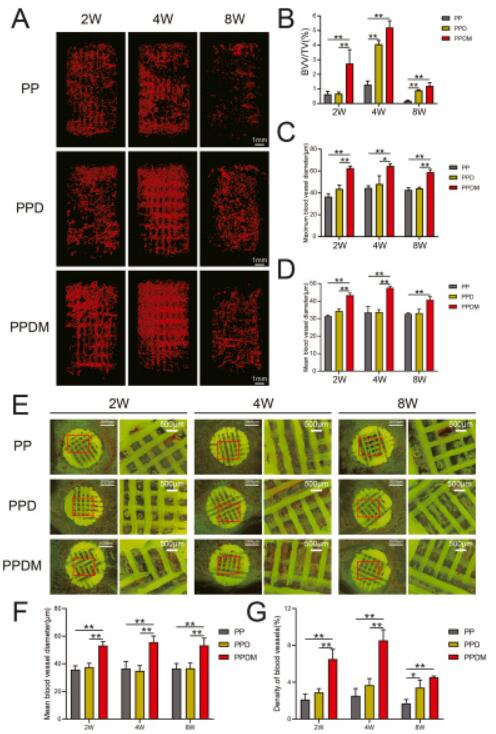
最后验证了PPDM支架在动物实验中的成骨和促血管生成的作用(图8)。从血管生成角度来讲,micro-CT显示PPDM支架内部血管更为成熟和连续,且PPDM组BVV/TV、血管直径和血管密度都高于其余样品。在硬组织切片中血管密度和血管直径测量中,也观察到类似情况,但植入8周后PPDM与PPD组血管密度差异不显著。
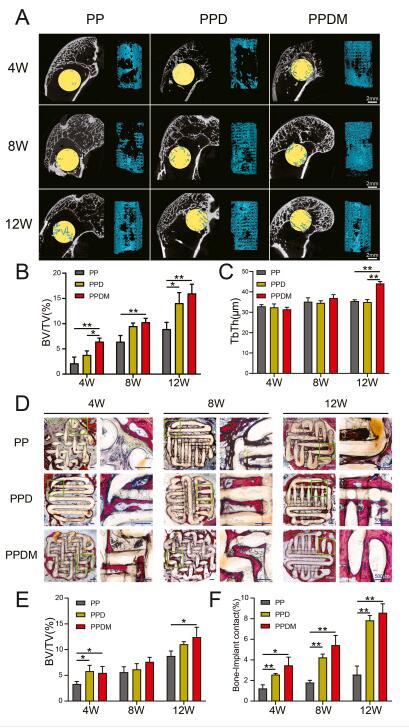
从体内骨整合实验角度分析(图9),多孔PEEK支架内骨向内生长的3D重建结果显示,植入早期(4周)PPDM组骨体积分数显著高于其余各组,12周后PPD与PPDM显著高于PP组;骨小梁厚度虽然在植入早期三组无明显差别,但12周后PPDM组显著高于其余各组。硬组织切片中显示在所有时间点,PPD组和PPDM组的骨组织与植入物接触始终高于PP组。结合PPDM组支架中的Mg2+释放曲线和体外促血管生成作用可以得出结论,PPDM组支架能够通过在植入后早期释放镁离子来促进多孔PEEK支架内的血管生长。
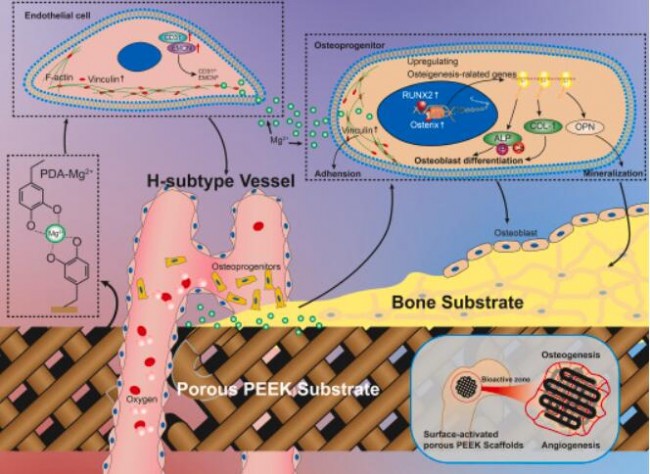 图10 镁表面活化的 3D 打印多孔PEEK支架促进血管生成和成骨的机制
图10 镁表面活化的 3D 打印多孔PEEK支架促进血管生成和成骨的机制
综上,研究团队证明3D打印多孔PEEK结构,并在其表面构建PDA-Mg2+生物活性涂层是一种提高生物惰性材料生物相容性的简便方法。含镁生物活性涂层改性的多孔聚醚醚酮支架在体外表现出优异的生物学功能,如促进细胞增殖和粘附、成骨分化和血管形成。
在体内实验中,PDA涂层显著改善了多孔PEEK支架的界面骨结合能力,而镁离子通过促进早期血管向内生长而增强了多孔PEEK支架内的骨向内生长能力(图10)。该方法为PEEK材料的临床应用提供了新的方法。
(责任编辑:admin)


 定向能量沉积(DED)金属3
定向能量沉积(DED)金属3 Sintavia获1000万美元新投
Sintavia获1000万美元新投 金属3D打印厂商汉邦激光启
金属3D打印厂商汉邦激光启 国家举办民营企业座谈会,
国家举办民营企业座谈会, 2025增材制造用户组(AMUG)
2025增材制造用户组(AMUG) 规划建设面积13.8万平方米
规划建设面积13.8万平方米 忍痛5年,福州依
忍痛5年,福州依 创想三维2023全球
创想三维2023全球 上海交大谷国迎教
上海交大谷国迎教 3D打印假体植入内
3D打印假体植入内 FRI:降脂油包水
FRI:降脂油包水 少年骨折后感染致
少年骨折后感染致

