牛津高性能材料公司3D打印医疗设备在日本获得批准
时间:2018-03-22 08:51 来源:中国3D打印网 作者:中国3D打印网 阅读:次
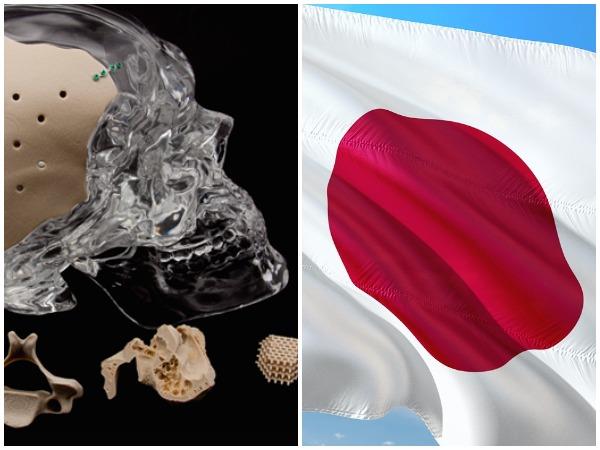
制作3D打印的医疗植入物,从设计它,然后采用正确的材料,进行必要的医学检测,这绝非易事,但对于一些医疗领域的公司来说,制造这样的设备实际上只是商业化道路上的一小步。这是因为,3D打印医疗设备需要得到政府机构的批准。在美国,FDA履行这一职责,检查个别产品,以确定它们是否符合人体使用的必要标准。
为此,FDA最近发布了关于医疗产品3D打印的指导,以便告诉制造商在产品中需要注意什么。
康涅狄格州的牛津高性能材料公司(OPM)是一家经常与FDA打交道的公司,旨在将其专门设计的PEKK(聚醚酮酮)医用植入物推向市场。该公司的OsteoFab植入物是业内最受欢迎的植入物,而且OPM在获得FDA(美国食品及药物管理局)510(k)许可,已经开发了几种不同的植入物。
但这是在美国,而其他市场呢?尽管一些国家对3D打印相对持怀疑态度,并且不急于批准可能出现问题的产品,当然也有一部分国家正在采取不同的措施。例如,在韩国,食品和药品安全部已经开发了3D打印医疗设备的快速选项,以加快技术的发展。当然,这是一种危险的策略,但它可以使国民经济受益。在亚洲的其他地区,日本仍然是医疗器械市场的一个有影响力的群体。对于OPM来说幸运的,日本厚生劳动省刚刚授予美国公司“国外医疗器械制造商认证”,允许其将激光熔化OsteoFab 3D打印医疗器械选件带到繁荣的亚洲国家。
牛津高性能材料公司首席执行官兼董事会主席Scott DeFelice表示:“10年前,OPM开始定期探索亚洲市场,以深入了解偿还环境,潜在市场和商业化机会。这一认证使OPM能够启动一项出口计划来启动市场开发并推动我们的亚洲业务。”
中国3D打印网译自:3ders.org 转载需注明出处!
(责任编辑:admin)
最新内容
热点内容


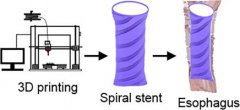 大西洋大学开发用于食道癌
大西洋大学开发用于食道癌 Ashley Furniture在制造过
Ashley Furniture在制造过 看美国研究人员如何继续改
看美国研究人员如何继续改 ITAMCO和普渡大学合作为美
ITAMCO和普渡大学合作为美 汉高收购美国一3D打印公司
汉高收购美国一3D打印公司 加拿大卫生部发布医疗设备
加拿大卫生部发布医疗设备

