世界首个3D打印定制五节长达19厘米脊椎 救治恶性脊椎肿瘤患者
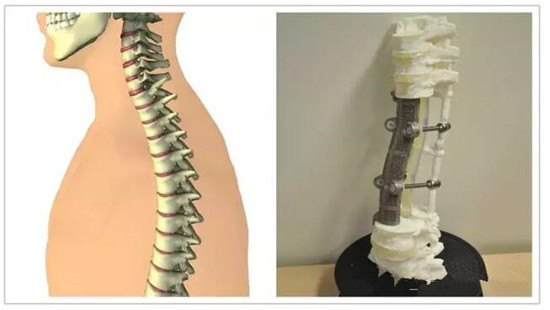
2016年6月12日早8点,北京大学第三医院骨科病房,患者袁先生平躺在手术室接诊车上。袁先生是一名恶性脊椎肿瘤――脊索瘤患者,肿瘤侵蚀五节脊椎,世界首个3D打印多节段胸腰椎植入物将在他的脊柱上完成长达19厘米的大跨度支撑,以替代被彻底切除的五节椎体。而这,在以往,是不可想象的。
前不久,CFDA(国家食品药品监督总局)批准注册了我国第一个也是全球首发的3D打印人工椎体产品,为我国3D打印技术在医学领域的应用起到重大推动作用。
患者袁先生所患为脊索瘤,是一种恶性肿瘤,长在胸椎和腰椎上,肿瘤侵犯范围非常广,胸椎10、11、12和腰椎1、2,共五节脊柱受到了侵蚀。这种情况,从医学上来说,除了通过手术把肿瘤切干净以挽救他外,别无它法。
手术本身也很困难,是一个罕见的疑难病例。可以切除五节脊椎的医院、医生,在世界上也寥寥无几。
据患者袁先生的主刀医生、此次获得CFDA注册认证的3D打印人工椎体研究团队负责人刘忠军教授介绍,按照目前通用的手术技术,即使切除五节椎体,接下来,要面临的就是,如何支撑?我们要使椎管内的脊髓和神经、血管等重要结构要保持完好的功能。但是,切除后,不要说功能,连可依附的脊椎结构都将不复存在。要对其结构、功能进行重建。最大的问题是将五节脊椎拿掉后,如何支撑?这对需切除五节脊椎的医生来说,遇到了前所未有的难题。
脊椎的固定技术大致分为前方和后方两种。后方的固定即便范围较大目前也能找到有效方式。因此对这个患者已经进行的一期手术时,切除了五节病变脊椎后方的结构,并采用椎弓根内固定技术在病变节段相邻上、下端的正常脊椎上拧入螺钉,将这些螺钉用金属棒连接固定便有了不错的强度,允许病人起床活动。
现在,前方的问题变成了老大难。将五节椎体完全拿掉本就需要超出常人的胆略,拿掉椎体后的大跨度支撑几乎没有现成方案。以往钛网内填入自体或异体碎骨是作为椎体间支撑的最常用器材,我们希望填充的碎骨与相邻的骨头能够长到一起,最终实现骨融合,完成稳定结构的重建。然而,单靠这种简单的支撑对这么大跨度结构重建可能不太靠谱,钛网一旦移位,压迫脊髓,患者就会瘫痪。再有,钛网呈笔直的圆柱状,与脊柱“S”形的生理曲线并不匹配。更令人尴尬的是,就算我们在别无可选的情况下仍决定用钛网,也没有厂家能够提供足够大规格的产品。因为这么大跨度的钛网支撑重建并无先例。
“有了3D打印技术,我们就多了一个选择。我们可以利用金属3D打印技术,依照患者的解剖结构,制造出一枚与五节椎体形态与长度相仿的人工椎体。人工椎体优势显著,首先,将其放到切除病变后的相邻椎体之间,能起到可靠的连接和支撑功能。同时利用金属3D打印人工椎体在结构上可以任意设计的便利,我们专门设计了其与后方内固定结构之间的连接,这种前后连成一体的装置使稳定性大大增强,在力学性能上可以说是质的飞越。有了这样的固定方式,术后很早期患者就可以下床活动。更特殊的优势是人工椎体被制成微孔结构,形状像海绵一样,类似我们骨头中的骨小梁。有了这种‘骨小梁’,相邻正常椎体的骨细胞可以长入其中,最终二者融为一体,从而实现骨整合。”刘忠军说。
5月6日,全球首发金属3D打印人体植入物――人工椎体获得CFDA注册批准。这标志着在3D打印植入物领域,我国已居世界领先水平。中国制造未来将造福更多患者。
获得注册的人工椎体产品,属于直接植入人体的三类骨科植入物,为我国监管等级最高的医疗器械产品。该产品是由北京大学第三医院骨科和北京爱康宜诚医疗器材股份有限公司合作开发研制。该团队研制的3D打印人工髋关节产品曾为我国首个获得CFDA注册批准的3D打印人体植入物于2015年获批,意味着3D打印植入物得到认可。
2009年,北京大学第三医院将3D打印技术引入骨科领域,经过跨学科、跨领域合作,历经多年的研制及临床观察,终于在他们手中诞生了世界首例3D打印人工椎体。
目前,经CFDA注册批准的3D打印人体植入物我国仅此两项。
“如果没有此技术,面对这名患者我们只能如实相告:抱歉,我们现在还无法为您找到理想的治疗方式,这个手术我们还做不了……对患者来说,这是一个难以接受的悲剧。在此次,利用3D打印技术按照患者的解剖结构,完成脊椎结构重建,完成内固定。装上这样一枚从形状到功能都与人体原本解剖结构相近的人造脊椎,患者最终可以挺起脊梁,像常人一样,正常工作,正常生活。”
手术顺利,6个多小时后,袁先生被推出手术室。由于术中出血量小,生命体征平稳,术后他未被推进ICU,而是直接回到了普通病房。

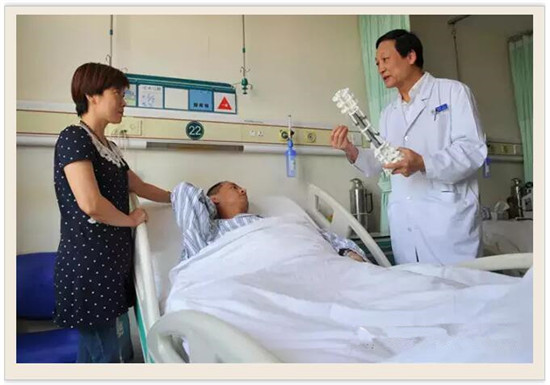
袁先生只是众多需要救治的患者之一。全球首发3D打印人工椎体在我国通过CFDA认证,意味着以前无计可施的患者有可以借助先进的技术得到施治,中国制造将造福更多的患者;产品国产化后也将打破国外产品对高端市场的垄断,大大降低价格,为患者节约大笔医疗支出;对推动整个3D打印产业链的发展具有里程碑式意义。
(责任编辑:admin)


 创想三维精彩亮相美国RAPI
创想三维精彩亮相美国RAPI 2019年中国技能竞赛“创想
2019年中国技能竞赛“创想 如何撬动消费升级带来的千
如何撬动消费升级带来的千 数字经济×千亿产业,催生
数字经济×千亿产业,催生 中南大学“创想杯”3D打印
中南大学“创想杯”3D打印 创想三维走进浙江科技学院
创想三维走进浙江科技学院 国际博物馆日,中
国际博物馆日,中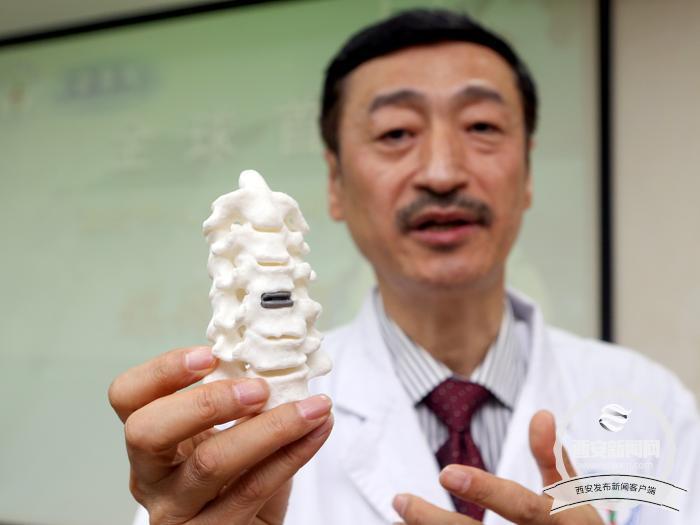 全球首例3D打印人
全球首例3D打印人 未来就是现在,工
未来就是现在,工

